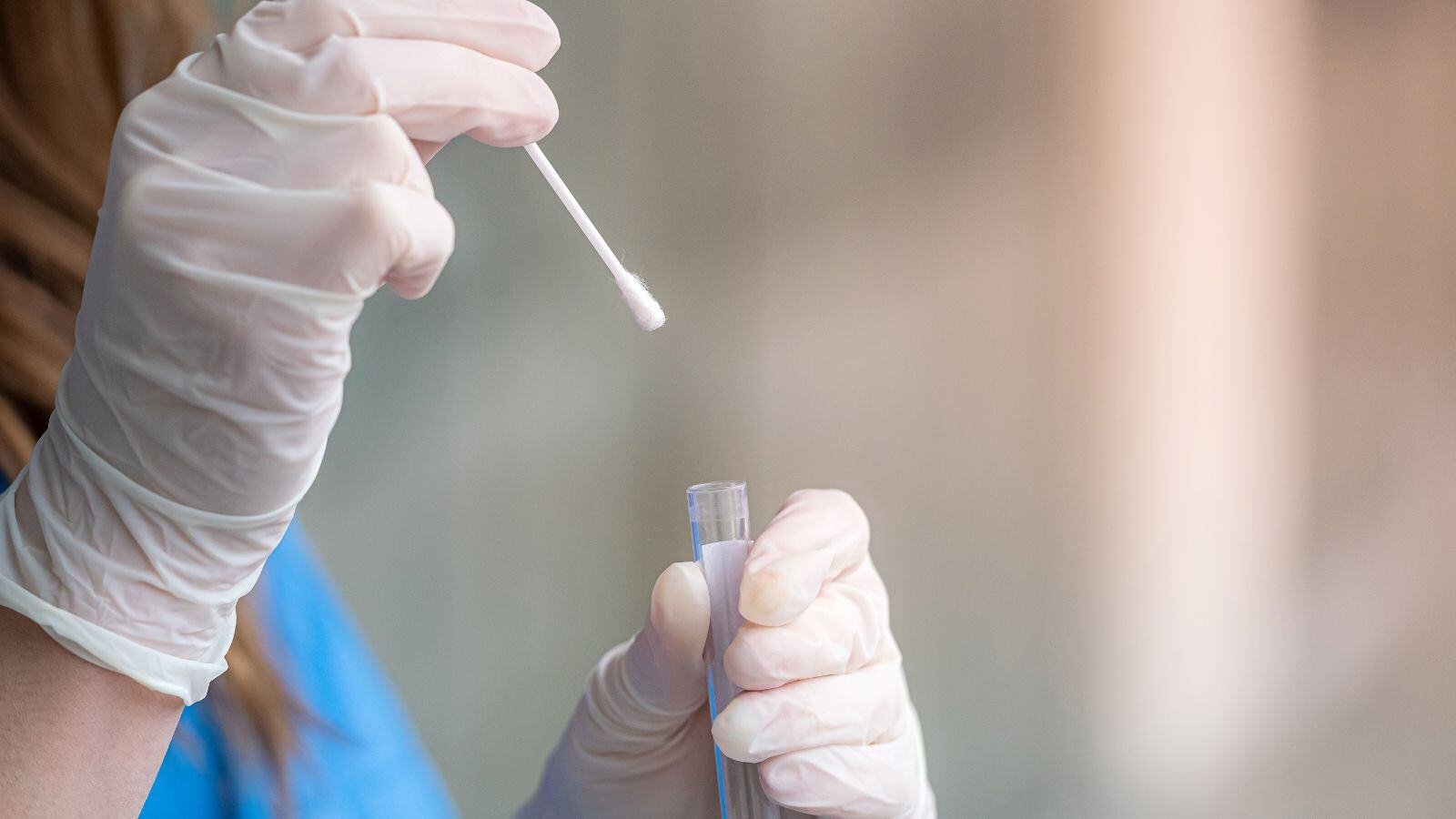
体外诊断
IVDR 合规专家,助力诊断创新
应对 IVDR 复杂性需要深厚的法规知识和实操经验。QbD Group 支持 IVD 制造商从产品开发到上市后合规,确保您的产品满足所有欧盟法规要求。
全面的 IVDR 支持
从差距评估到公告机构提交,我们的专家指导您完成 IVDR 合规的每一步。
IVD 专用临床服务
凭借在超过 45 种分析物中完成 280+ 项临床性能研究的经验,我们为 IVD 提供量身定制的临床服务。
集成的 CDx 专业知识
我们支持伴随诊断全生态系统 — 从生物标志物策略和分析验证到法规提交和上市后随访。
端到端质量保证
ISO 13485 实施、QMS 整改和持续合规支持,根据您的 IVD 产品组合量身定制。
Tailored solutions
Our solutions for 体外诊断
Explore purpose-built solutions designed to address the specific regulatory, quality, and compliance challenges in your industry.
Cross-industry solutions
Lifecycle
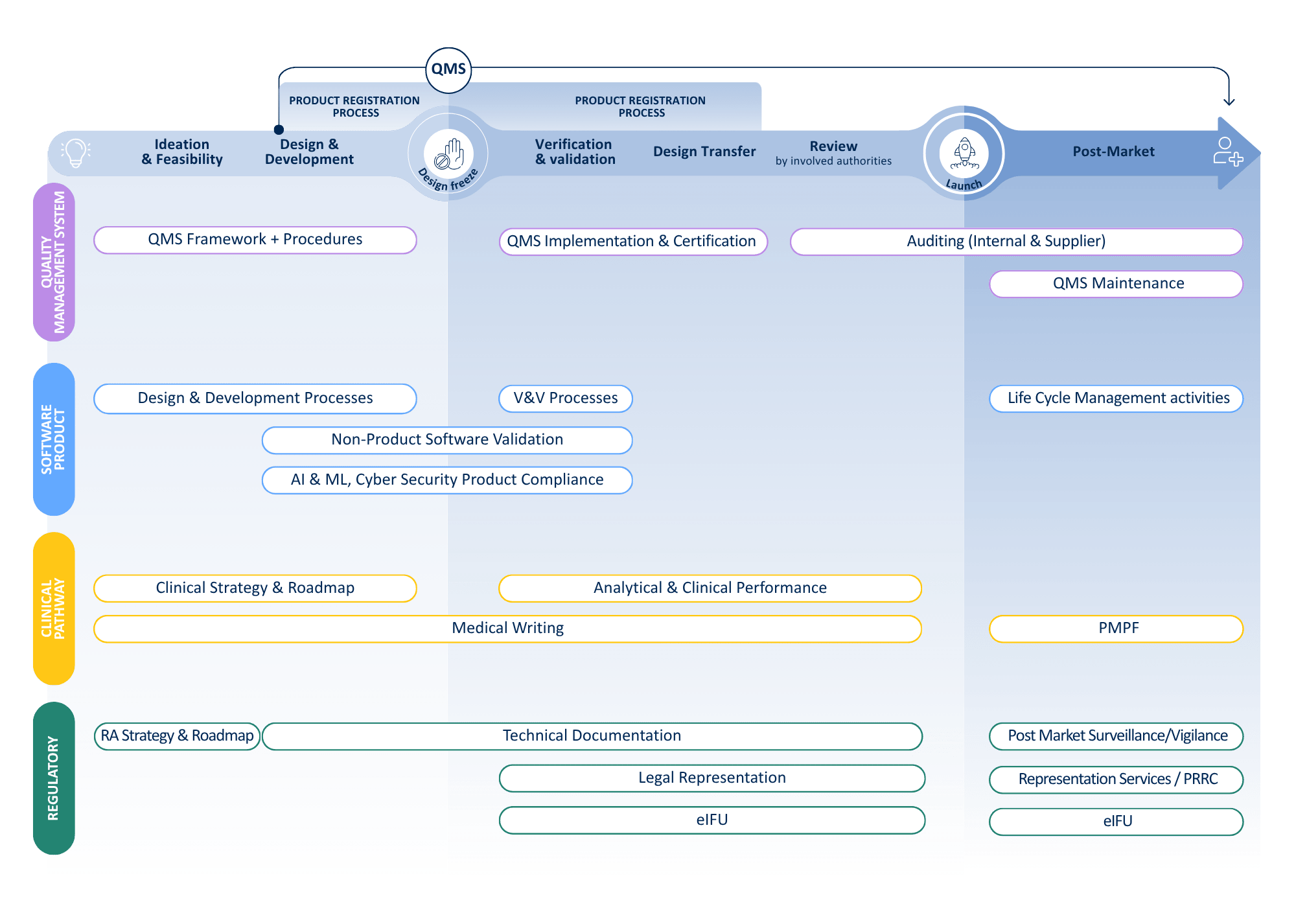
Product lifecycle
从概念到上市后随访 — 我们为 IVD 制造商在 IVDR 合规之旅的每一步提供支持。
Industry context
Industry challenges
These are the realities shaping your industry — and exactly where our specialists make a difference.
IVDR 过渡复杂性
从 IVDD 到 IVDR 的过渡引入了基于风险的分类、更严格的临床证据要求和强制性公告机构参与。
临床证据生成
证明科学有效性、分析性能和临床性能需要结构化的研究设计和特定 IVD 的专业知识。
创新与合规的平衡
人工智能、快速检测和数字 IVD 等新兴技术带来了独特的法规挑战,需要灵活的合规策略。
伴随诊断法规路径
CDx 需要与治疗药物开发协调一致的法规策略,跨越多个利益相关方和法规框架。
Our services
How we can help you4

为什么选择QbD Group
您值得信赖的合作伙伴
QbD Group 拥有专门的 IVD 团队,结合法规、临床和质量专业知识,帮助 IVD 制造商在 IVDR 下成功运营。凭借对 IVD 领域的深入了解和丰富经验,我们提供实用、可操作的解决方案。
IVD 专属专业知识
不同于通用法规咨询,我们拥有专门的 IVD 团队和专业知识。
280+ 项临床性能研究
在超过 45 种分析物中拥有丰富经验,覆盖多种分类。
IVDR 先行者
在 IVDR 过渡的前沿,帮助企业未雨绸缪。
集成的 CDx 能力
通过 PrecisionDx™ 提供跨整个 CDx 生态系统的独特支持。
常见问题
常见问题





