医疗器械
从创意到患者 — 每个阶段的专家支持
寻找医疗器械的质量、法规或临床支持?QbD Group 可以在医疗器械生命周期的任何阶段为您提供帮助,从创意到患者。我们是 ISO 13485、临床评估/调查、MDR、设计与开发、技术文件、审计、确认、验证、风险管理、软件等方面的专家。
全生命周期支持
QbD Group 在医疗器械生命周期的每个阶段提供专家指导,从概念到患者,确保合规和市场成功。
值得信赖的法规专业知识
凭借对 ISO 13485、MDR 和风险管理的深入了解,我们帮助您应对复杂法规,安全有效地将器械推向市场。
全面的质量与临床解决方案
从质量管理体系的实施到临床评估和调查的执行,QbD Group 确保您的医疗器械达到最高的安全和性能标准。
上市后监控与维护
我们通过管理上市后监控以及维持医疗器械安全性和有效性所需的流程来支持持续合规。
Tailored solutions
Our solutions for 医疗器械
Explore purpose-built solutions designed to address the specific regulatory, quality, and compliance challenges in your industry.
Cross-industry solutions

从创意到患者的伙伴
无论您是在准备 CE 标志、应对 MDD 到 MDR 的过渡,还是扩展上市后监控 — 我们的专家在医疗器械生命周期的每个阶段为您提供指导。
Lifecycle
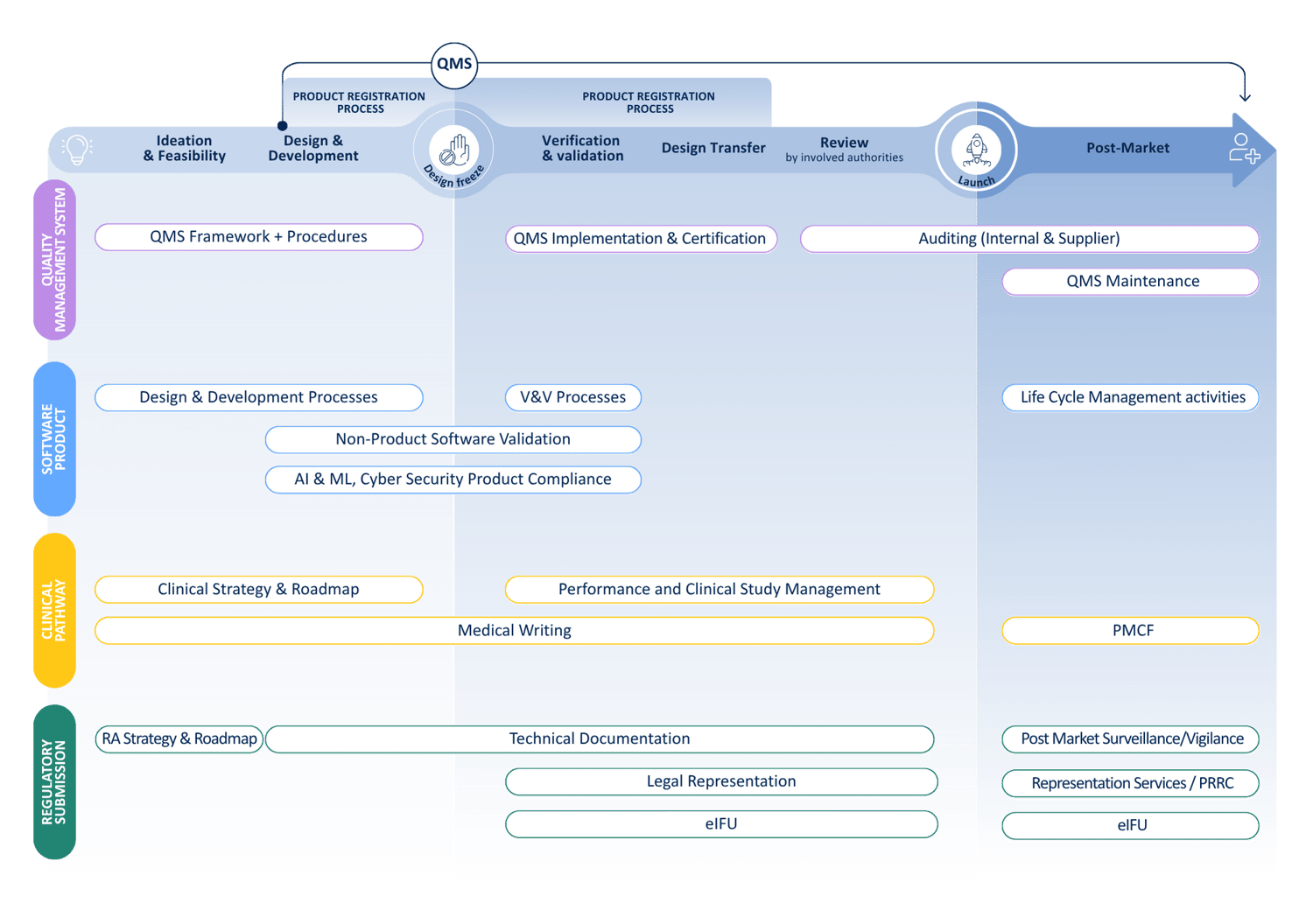
Product lifecycle
每个阶段的伙伴 — 从概念和法规策略到上市后合规,我们支持医疗器械的全生命周期。
Our services
How we can help you4
质量保证
- FDA、EMA、FAHMP 和 ISO 标准(ISO 13485、ISO 14971 等)的实施。
- 经认证的主任审核员进行内部和外部审核。
- 医疗器械软件生命周期管理和数字健康解决方案。
软件解决方案与服务
- 符合 IEC 62304 的软件生命周期合规和设计开发支持。
- SaMD 分类、AI 法案准备和网络安全评估。
- DevOps 与 QMS 集成,实现优化的软件发布。
Services
Featured12

为什么选择QbD Group
您值得信赖的合作伙伴
在 QbD Group,我们结合深厚的法规、临床和质量专业知识,帮助医疗器械制造商、分销商和进口商在整个医疗器械生命周期中满足法规要求。从全套临床研究到技术文件,我们的专家在 MDR 认证过程的每个阶段为您提供支持。
获得公告机构认可
我们的工作质量得到行业领先认证机构的认可。
全球公认的 MDR 专家
在 MDR、IVDR 和国际法规方面拥有深厚的专业知识。
10年以上经验
在支持各种规模的医疗器械公司方面拥有卓越的业绩记录。
行业领先
我们走在法规变化的前沿,让您能够专注于创新。
常见问题
常见问题