Productos combinados fármaco-dispositivo
Navega las vías regulatorias de la UE y EE. UU. con confianza
Navegar las vías regulatorias a menudo puede sentirse como un laberinto, llevando a incertidumbre y posibles errores en el proceso de presentación. Esto es aún más cierto cuando se trata de productos combinados. En QbD Group, ofrecemos soluciones integrales para navegar el complejo proceso de registro de estos productos innovadores tanto en la Unión Europea (UE) como en Estados Unidos (EE. UU.).
Marco regulatorio
En Europa, los productos combinados se regulan según su Mecanismo de Acción Principal (PMOA) — si el producto actúa principalmente como producto medicinal o como dispositivo médico. Esto determina qué vía regulatoria aplica.
Desafíos clave que abordamos
Identificación del PMOA
Determinar el Mecanismo de Acción Principal define la vía regulatoria completa y el dossier requerido.
Clasificación cruzada
Los productos combinados operan entre marcos de fármacos y dispositivos, requiriendo coordinación regulatoria dual.
Marcos regulatorios diferentes
La UE y EE. UU. aplican enfoques fundamentalmente diferentes para la clasificación y aprobación de productos combinados.
Requisitos de presentación complejos
Los dossiers regulatorios integrados deben satisfacer a múltiples autoridades.
Productos combinados liderados por el dispositivo
Si tu producto está clasificado como dispositivo médico con una sustancia medicinal auxiliar, debe cumplir con el MDR 2017/745 de la UE.
Ejemplos
Stent liberador de fármaco → Vía de dispositivo (MDR + opinión EMA)
Catéter recubierto → Vía de dispositivo (MDR)
Productos combinados liderados por el producto medicinal
Si tu producto es principalmente un producto medicinal, la combinación se regula bajo la Directiva de Productos Medicinales (2001/83/CE).
Ejemplos
Jeringa precargada → Vía de fármaco (DPM)
Parche anticonceptivo → Vía de fármaco (DPM)
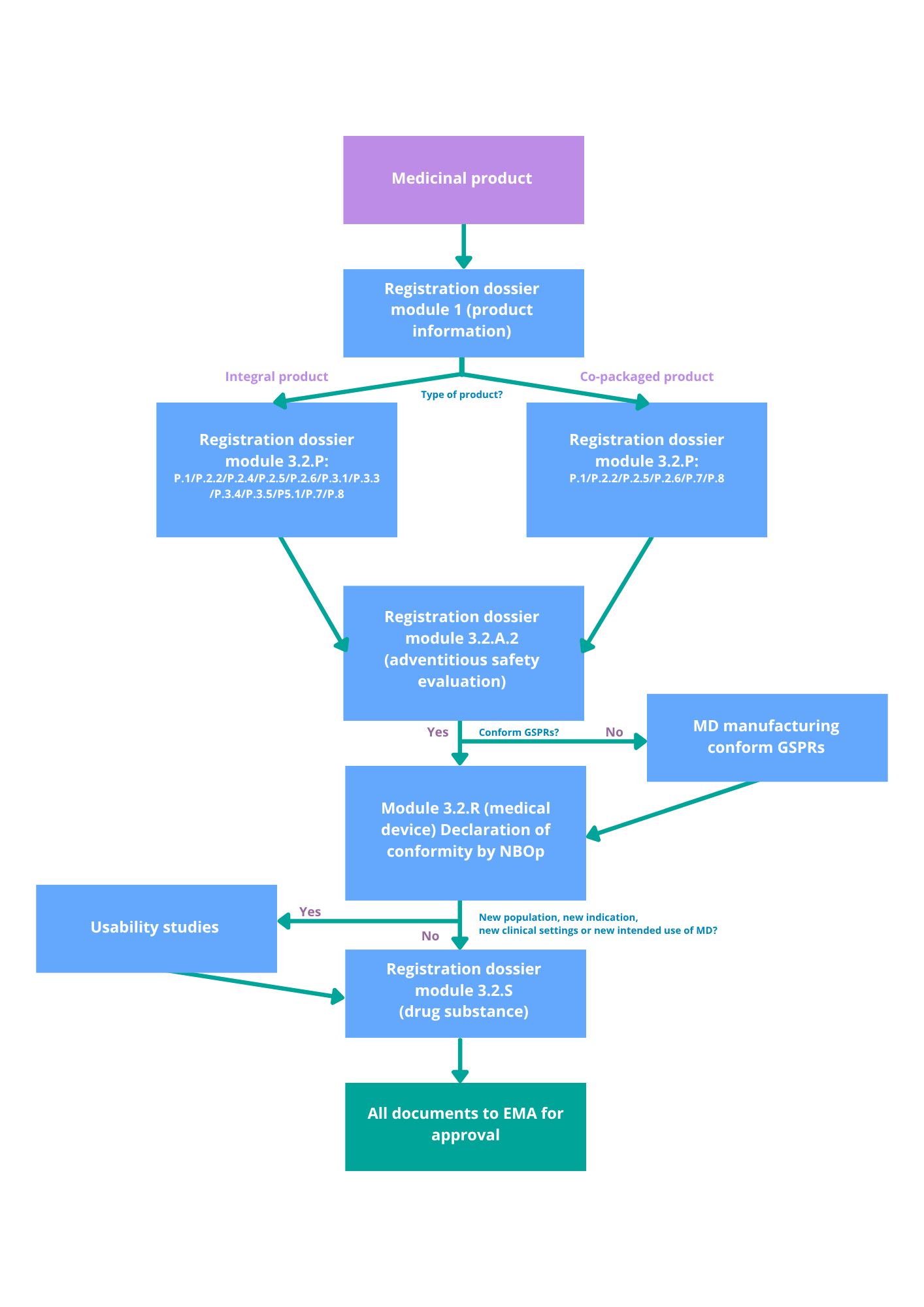
Nuestro enfoque estructurado
Identifica el centro líder de la FDA
Determina el Mecanismo de Acción Principal (fármaco, dispositivo o biológico). Si no está claro, presenta una Solicitud de Designación (RFD) a la FDA.
Determina la solicitud de investigación
Dependiendo del PMOA, solicita un IND cuando el modo principal es fármaco o biológico, o un IDE cuando es dispositivo.
Selecciona la solicitud de comercialización
Liderada por fármaco: NDA o ANDA. Liderada por biológico: BLA. Liderada por dispositivo: PMA, De Novo o 510(k).
Gestión del ciclo de vida poscomercialización
Mantén el cumplimiento continuo en ambos marcos regulatorios.
Nuestras soluciones integradas
Nuestras soluciones integradas apoyan a las organizaciones a lo largo de todo su ciclo operativo, desde actividades de cumplimiento hasta control sostenido, mejora y habilitación digital.
Lo que obtienes
Estrategia regulatoria a medida
Te ayudamos a desarrollar una hoja de ruta regulatoria personalizada.
Orientación experta en procedimientos
Nuestro equipo te guía en la selección del procedimiento regulatorio más adecuado.
Gestión integral del ciclo de vida
Desde el concepto hasta el lanzamiento al mercado, ofrecemos soporte holístico.
Profundo conocimiento regulatorio
Aprovecha nuestro amplio expertise para navegar requisitos estrictos con confianza.
Por qué QbD Group
Tu socio de confianza
Expertise transversal
nuestros especialistas regulatorios cubren Pharma, Biotech, Medical Devices, IVD y Productos Combinados bajo un mismo techo.
Planificación regulatoria estratégica
alineamos tu vía regulatoria con los objetivos comerciales para acelerar el time-to-market.
Historial probado
con miles de presentaciones exitosas y proyectos de gestión de dossiers en toda Europa.
Soporte escalable
desde una consulta regulatoria puntual hasta operaciones regulatorias completas externalizadas.
FAQ
Preguntas frecuentes
Contenido relacionado
Ver todo
¿Tienes preguntas sobre las vías regulatorias para tu producto combinado?
Entendemos las complejidades de navegar las regulaciones de la UE y EE. UU. Nuestros expertos están aquí para ayudarte.