Regulatory Affairs
Tu experto regulatorio en Europa
Lleva tu producto al mercado con confianza gracias al soporte experto en Regulatory Affairs. Desde la estrategia hasta la aprobación del producto, ofrecemos servicios personalizados para navegar requisitos complejos y cumplir con los estándares europeos. Ya sea compilar expedientes técnicos, gestionar dossiers o coordinar con organismos reguladores, nos encargamos de los detalles para que tú puedas centrarte en la innovación.
Experiencia en Pharma y Biotech
Profundo conocimiento regulatorio para productos farmacéuticos y biotecnológicos en el mercado europeo.
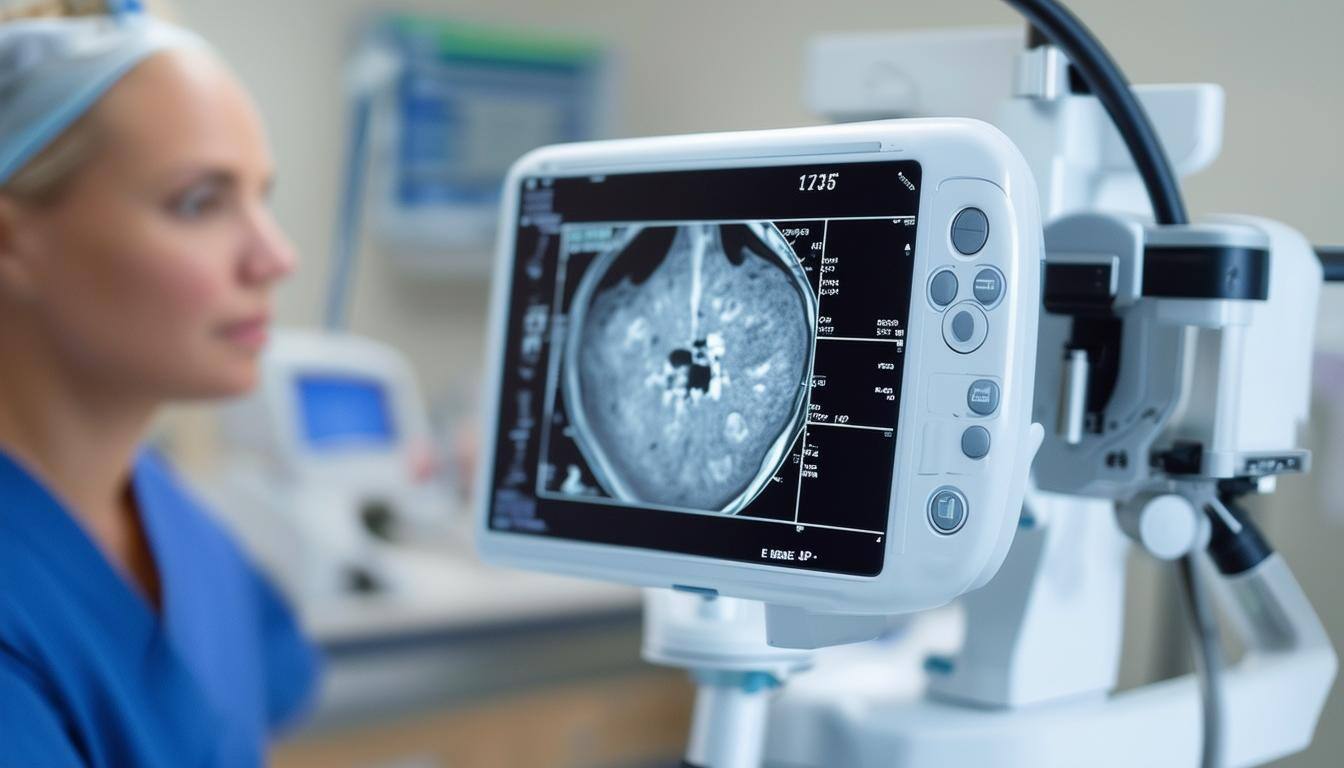
Dominio en dispositivos médicos
Orientación experta en requisitos MDR, documentación técnica e interacciones con organismos notificados.
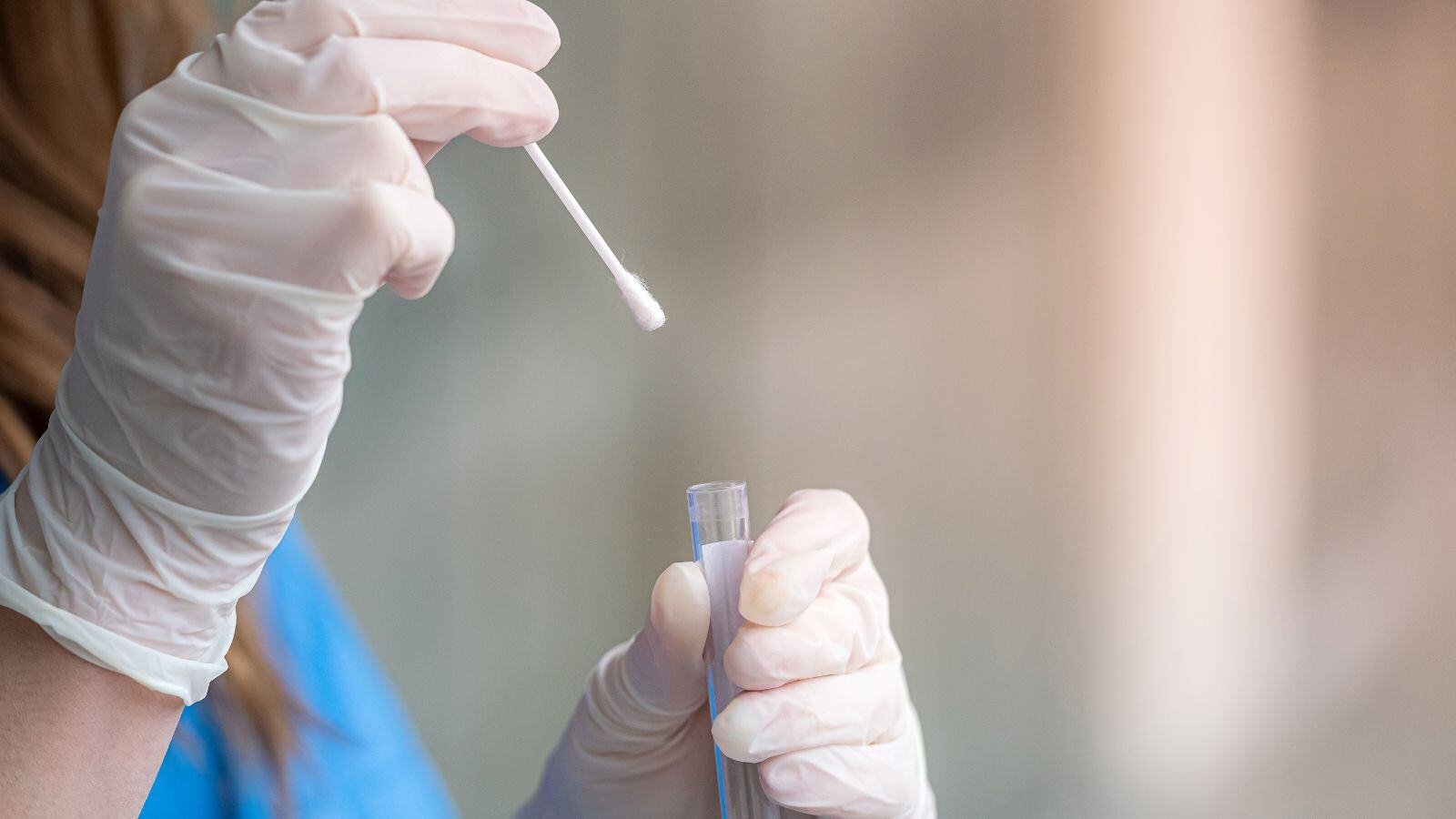
Soporte regulatorio para IVD
Soporte integral para el cumplimiento del IVDR, desde la clasificación hasta la evaluación del rendimiento y el lanzamiento al mercado.
Orientación en productos combinados
Navega el complejo panorama regulatorio de los productos combinados con nuestra experiencia multifuncional.
Nuestros servicios
Regulatory Affairs por industria

Por qué QbD Group
Tu socio de confianza
El equipo de Regulatory Affairs de QbD Group combina una profunda experiencia en la industria con un enfoque pragmático y práctico. Ayudamos a las empresas de Life Sciences a navegar eficientemente los complejos panoramas regulatorios europeos, desde la estrategia inicial hasta el cumplimiento post-comercialización.
Experiencia multisectorial: nuestros especialistas regulatorios cubren Pharma, Biotech, dispositivos médicos, IVD y productos combinados bajo un mismo techo.
Planificación regulatoria estratégica: alineamos tu ruta regulatoria con tus objetivos comerciales para acelerar el time-to-market.
Trayectoria demostrada: con miles de presentaciones exitosas y proyectos de gestión de dossiers en toda Europa, ofrecemos resultados de confianza.
Soporte escalable: desde una consulta regulatoria puntual hasta operaciones regulatorias completamente externalizadas, nos adaptamos a tus necesidades.